推荐阅读
黄荷凤院士课题组揭示胚胎源性疾病免疫学新机制

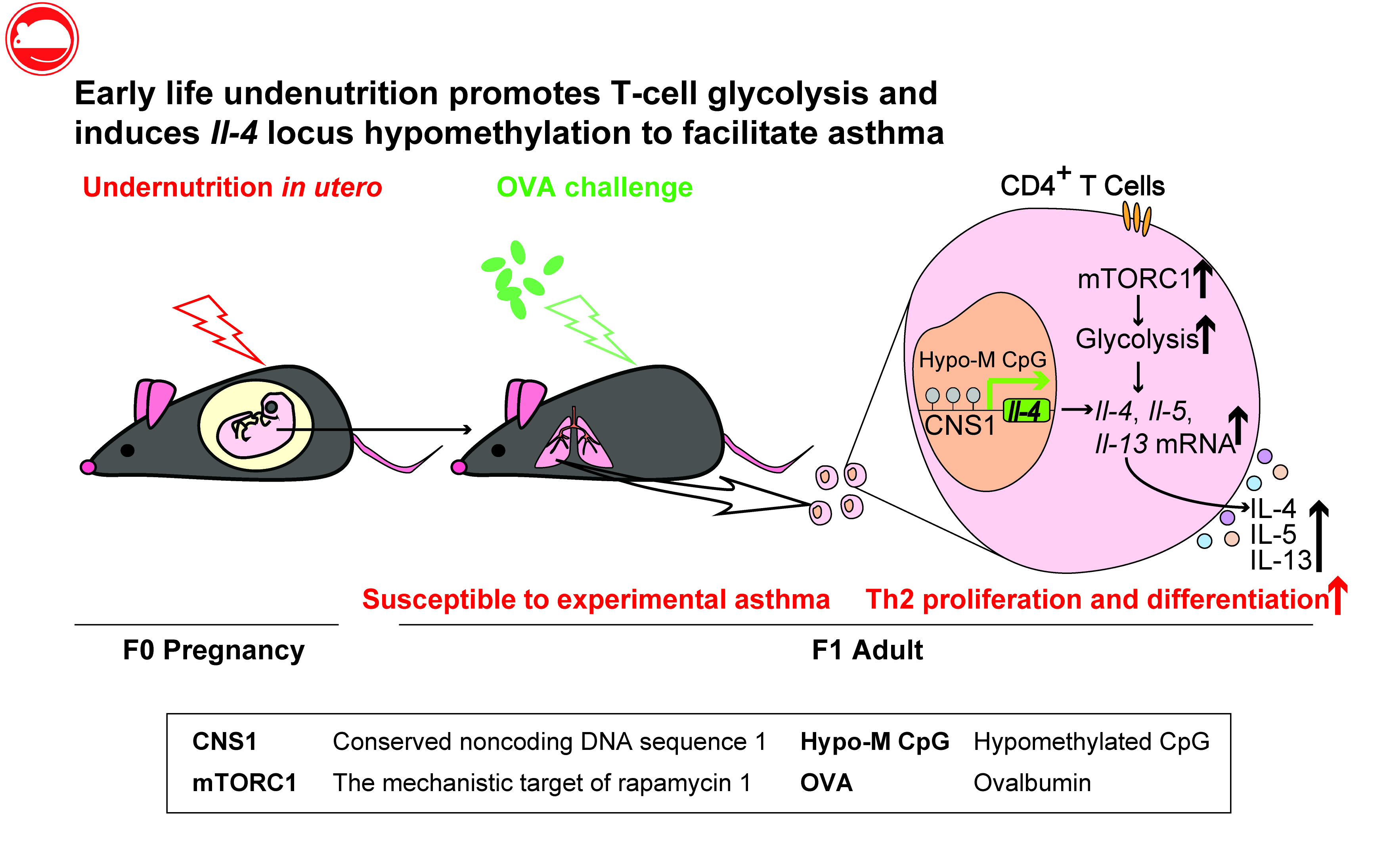
近日,上海交通大学医学院附属国际和平妇幼保健院、上海市胚胎源性疾病重点实验室黄荷凤院士领衔的研究团队在胚胎源性疾病方面的研究又取得了重要新发现,在The Journal of Allergy and Clinical Immunology(影响因子13.258)在线发表了题为Early life undernutrition reprograms CD4+T-cell glycolysis and epigenetics to facilitate asthma的研究论文,该研究利用生命早期营养不良小鼠模型,揭示了生命早期营养状况通过对小鼠免疫细胞的代谢水平以及表观遗传学的调控来影响其功能,最终影响了子代哮喘的发病。该研究为胚胎源性疾病机制的探索提供了新的思路和视角,为生命早期营养不良所致的哮喘易感性提供潜在的干预策略。
成人疾病的配子胚胎起源性是指在生命早期的配子胚胎发育过程中,母体内环境的不良改变可以导致其子代出生后患代谢性疾病如心血管病、糖尿病、肿瘤风险增加。最新的流行病学调查发现,胎儿宫内生长受限可以影响子代呼吸系统的发育和功能,并显著增加从儿童到成人哮喘发生风险,但其发生机制尚不清楚。
研究人员通过蛋白质限制来模拟营养不良的状态,构建了生命早期营养不良的小鼠模型,待子代成年后给予其肺部过敏原激发,发现生命早期营养不良的小鼠较生命早期营养正常的小鼠实验性哮喘易感。而这一哮喘易感性表现出一定的性别差异,在雌性子代中没有发现哮喘加重的迹象,这可能与发育源性疾病存在性别偏好有关。值得关注的是,研究人员发现母体妊娠期即子宫内的营养状况相较于哺乳期的营养状况对子代实验性哮喘易感性影响更大。这也提示准妈妈们更要注重妊娠期的营养水平和营养均衡。
CD4+T淋巴细胞在过敏性哮喘发病中发挥了关键作用。研究人员发现无论是在体外诱导刺激条件下还是哮喘模型中,生命早期营养不良的小鼠CD4+T淋巴细胞的活化和增殖较生命早期营养正常的小鼠显著增强,且更易向Th2型细胞分化。CD4+T淋巴细胞的功能和命运决定受代谢水平和表观遗传修饰的严密调控。研究人员利用Seahorse能量测定仪的代谢分析等技术,发现生命早期营养不良的小鼠CD4+T淋巴细胞活化后表现出更强的糖酵解速率,而氧化磷酸化速率没有发生显著改变。重要的是,当阻断糖酵解途径之后,生命早期营养不良小鼠的CD4+T淋巴细胞的功能和分化水平被显著抑制,实验性哮喘症状也得到明显缓解。此外,该研究还发现生命早期营养不良会诱导CD4+T淋巴细胞二型细胞因子基因位点的低甲基化,使得CD4+T淋巴细胞更易于向Th2型细胞分化。该研究阐明了母体妊娠期的营养状况会通过重塑子代免疫细胞自身的代谢和表观遗传修饰水平来调控其功能和命运决定,最终影响子代成年后的哮喘发病,这也为其他成年性疾病发育起源的研究提供了新的思路。
上海交通大学医学院博士后陈茜博士和博士研究生林慧为该论文并列第一作者,上海交通大学医学院附属国际和平妇幼保健院黄荷凤院士、刘欣梅副研究员、浙江大学盛建中教授为该论文共同通讯作者。该工作还得到了北京师范大学生命科学学院刘光伟教授、复旦大学医学院徐薇副教授的大力支持和帮助。
